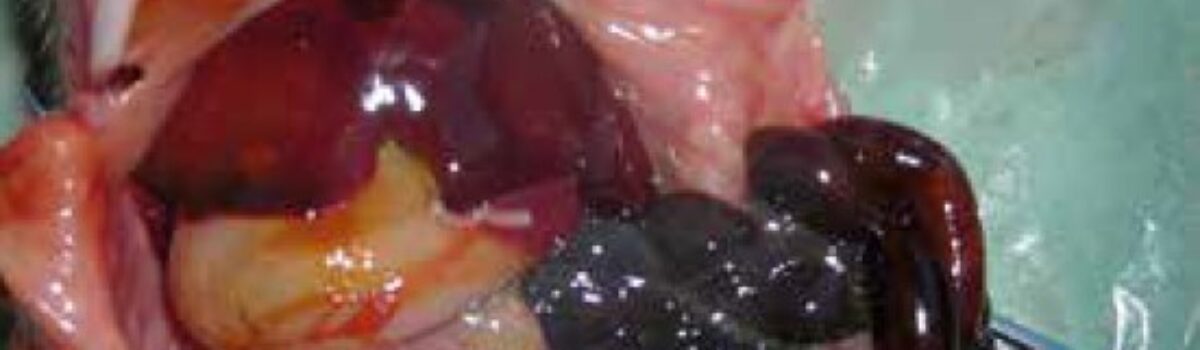
Beztlenowce oraz Lawsonia intracellularis – niedoceniane przyczyny zachorowań prosiąt
Zygmunt Pejsak
Wydział Medycyny Weterynaryjnej
Uniwersytet Rolniczy w Krakowie
Beztlenowce oraz Lawsonia intracellularis – niedoceniane przyczyny zachorowań prosiąt
W maju (21-23.05) bieżącego roku odbyło się w Bernie (Szwajcaria) kolejne Europejskie Sympozjum Zarządzania Zdrowiem Świń ( European Symposium of Porcine Health Management – ESPHM).
Spotkania tego rodzaju przeznaczone są dla lekarzy weterynarii zajmujących się ochroną zdrowia świń. Organizowane są w Europie w odstępach jednego roku. Poprzednie miało miejsce w Lipsku. Do Berna przybyli lekarze weterynarii z krajów Europy, ale także z wielu państw świata, praktycznie ze wszystkich kontynentów. W sumie w sympozjum wzięło udział 1028 uczestników. Z Polski uczestniczyło w nim 45 lekarzy weterynarii.
Analizując tematykę zgłoszonych na kongres prac można uznać, że wyjątkowo dużo dotyczyło dobrostanu zwierząt. Pojawiło się szereg doniesień związanych z organizacją i zarządzaniem produkcją świń. Coraz więcej zaprezentowanych doniesień związanych było ze zintegrowaną opieką weterynaryjną nad stadami świń. Sporą grupę stanowiły prace dotyczące precyzyjnego chowu świń. Szereg traktowało o możliwości wykorzystania sztucznej inteligencji (AI) w zarządzaniu chowem świń.
Było też kilkanaście prac opisujących wpływ globalnego ocieplenia na produkcję zwierzęcą oraz możliwości oddziaływania na skład mikrobiomu jelit, szczególnie w okresie poodsadzeniowym.
Temu zagadnieniu poświęcony będzie kolejny artykuł, prezentujący dane, jakie przedstawiono na ten temat w Bernie.
W niniejszym postanowiono zwrócić uwagę na ważne w etiologii biegunek prosiąt, aczkolwiek ciągle niedocenianie w tym aspekcie beztlenowce i drobnoustroje Lawsonia (L) intracellularis, o czym też mówiono w Bernie. Beztlenowce na pewno nie są główną przyczyną biegunek prosiąt, ale mogą odgrywać ważną rolę jako czynniki współtowarzyszące w ich powstawaniu, szczególnie u prosiąt ssących. Z kolei L. intracellularis kojarzona jest głównie z problemami u tuczników i starszych warchlaków. Okazuje się, że problem dotyczyć może także prosiąt powyżej 7-8 tygodnia życia.
Przyczyną rozprzestrzenienia i jednocześnie niedoceniania znaczenia beztlenowców w etiologii biegunek są przede wszystkim właściwości biologiczne tych drobnoustrojów utrudniające w sposób zdecydowany diagnostykę laboratoryjną.
Beztlenowce należą do najstarszych filogenetycznie drobnoustrojów (najbardziej prymitywnych), w związku z czym są dobrze zaadaptowane do składu atmosfery Ziemi, która w swoim czasie była pozbawiona tlenu, natomiast zasobna była w wodór i azot. Z tego powodu ich najważniejszą cechą jest wrażliwość na działanie tlenu.
Beztlenowce tworzą dwie grupy całkowicie odmiennych bakterii. Jedne z nich (rodzaj Clostridium) zdolne są do wytwarzania endospor (spor – przetrwalników) – beztlenowce sporulujace, a inne (m.in. Fusobacterium i Brachyspira) są tej cechy pozbawione. Przetrwalniki stanowią formę przystosowania organizmów do niesprzyjających warunków środowiskowych. Kiedy warunki zewnętrzne stają się korzystne, przetrwalnik absorbuje wodę, rozrywa okrywę zewnętrzną i przekształca się w normalną komórkę bakteryjną. Spory umożliwiają niektórym beztlenowcom sporulujacym przeżycie co najmniej 30 lat.
Za podstawowe źródło bytowania Clostridium (C.) uważany jest przewód pokarmowy zwierząt i człowieka oraz ziemia (w znaczeniu gleby). Można uznać, że beztlenowce są normalną składową mikrobiomu przewodu pokarmowego. Co więcej, beztlenowce stanowią jego zasadniczy, stabilizujący składnik. Przykładowo, beztlenowce z gatunku (Bacteroides spp.) są producentem krótkołańcuchowych kwasów tłuszczowych (SCFA), między innymi maślanów. Te ostatnie stanowią podstawowe źródło energii dla komórek jelitowych. Niepatogenne beztlenowce z gatunku Clostridium spp. wspomagają trawienie niestrawionych resztek pokarmowych np. błonnika. Na zasadzie tak zwanej konkurencji wypierającej (competitive exclusion) chronią przewód pokarmowy przed zasiedleniem go bakteriami bezwzględnie chorobotwórczymi. Niektóre gatunki beztlenowców (Prevotella spp.) uczestniczą w metabolizmie węglowodanów. Można stwierdzić, że beztlenowce wspomagają trawienie, odporność i zdrowie jelit. Prawidłowe funkcjonowanie przewodu pokarmowego zależne jest od obecności w nim odpowiedniej ilości i liczby gatunków beztlenowców.
Niestety, niektóre gatunki beztlenowców, w przypadku gdy stworzone zostaną dla nich optymalne warunki do intensywnego namnażania, mogą stać się współodpowiedzialne za pojawienie się biegunek. Ma to miejsce przede wszystkim w odniesieniu do prosiąt noworodków oraz rzadziej – prosiąt ssących.
W patologii świń szczególną rolę odgrywają laseczki z rodzaju Clostridium. Drobnoustroje te wykazują dużą oporność na niekorzystne oddziaływanie warunków środowiskowych (wysokie, niskie temperatury, wysuszenie, wpływ tlenu itd.). W środowisku zewnętrznym zachowują żywotność zaskakująco długo. Dla przykładu C. chouvei kilkanaście lat.
Problem chorób świń wywoływanych przez beztlenowce wydaje się mieć narastające znaczenie praktyczne. Jak już wspomniano, zagadnienie to jest jak dotychczas niełatwe do diagnostyki laboratoryjnej ze względu na niepełną wiedzę odnośnie zróżnicowanych właściwości biologicznych beztlenowców. Wysoce odmienny jest również obraz kliniczny i sekcyjny zakażeń świń. Zróżnicowanie objawów chorobowych i zmian sekcyjnych wywołanych przez różne beztlenowce związane jest z aktywnością wytwarzanych przez nie toksyn oraz innych – bakteryjnych, wirusowych i pasożytniczych – czynników chorobotwórczych biorących udział w etiologii biegunek. Istotą chorób wywołanych przez beztlenowce jest niezwykłość etiopatogenezy polegająca na tym, że występujący w odrębnych serotypach jeden gatunek bakterii np. C. pefringens wywołuje bardzo różne procesy chorobowe, które przebiegają przeważnie gwałtownie, powodując nagłe padnięcia zwierząt.
Rozpoznanie laboratoryjne chorób beztlenowcowych komplikuje fakt, że wykrycie drobnoustroju nie pozwala na wyrażenie opinii odnośnie jego udziału w etiologii choroby (ogromna większość beztlenowców nie posiada właściwości chorobotwórczych). Ostateczną diagnozę można postawić dopiero po określeniu zdolności bakterii do wytwarzania poszczególnych toksyn oraz określeniu typu toksyn. Warto jednocześnie pamiętać, że niektóre gatunki beztlenowców wytwarzają kilkanaście różnych toksyn i tylko niektóre z nich są chorobotwórcze.
Oceniając wynik badania laboratoryjnego należy pamiętać o tym, że wiele różnych gatunków beztlenowców może występować w przewodzie pokarmowym u świń zdrowych, niewykazujących żadnych objawów chorobowych.
Do beztlenowców chorobotwórczych zaliczyć należy przede wszystkim Clostridium perfringens typu C oraz beztlenowce z gatunku Clostridium difficile.
Pierwszy wymieniony gatunek odpowiedzialny jest za krwotoczne zapalenie jelit noworodków świń. Drugi jest częstym „udziałowcem” biegunek, przede wszystkim, prosiąt ssących, a niekiedy także odsadzonych.
Krwotoczne zapalenie jelit noworodków wywołane przez C. perfringens typu C
Czynnik etiologiczny omawianej choroby C. perfringens typu C zaliczyć należy do normalnego składu mikrobiomu przewodu pokarmowego świń; jako drobnoustrój niechorobotwórczy.
Do zasiedlenia przewodu pokarmowego prosiąt noworodków dochodzi w kojcu porodowym, do którego beztlenowce wysiewane są najczęściej z kałem loch. W przewodzie pokarmowym prosiąt noworodków pod wpływem sprzyjających okoliczności, jak np. braku odporności swoistej oraz niskiego poziomu higieny – z czym związana jest intensywność zasiedlania – następuje ich szybkie i intensywne namnożenie. Jednocześnie ma miejsce eliminacja innych gatunków bakterii normalnej flory jelitowej. Konsekwencją jest wytwarzanie dużej ilości toksyny beta, która jest głównym czynnikiem chorobotwórczości – w przebiegu omawianej jednostki chorobowej. Toksyna ta prowadzi do wystąpienia objawów ogólnych u prosiąt noworodków do 5 dnia życia, najczęściej między 1 a 3 dniem. Choroba występuje rzadko u prosiąt powyżej 7 dnia życia. Obserwuje się krwotoczną, nagle pojawiającą się biegunkę, oraz liczne zejścia śmiertelne. Toksyna ta jest wrażliwa na działanie proteaz, dlatego rzadko stanowi problem kliniczny u prosiąt starszych. Inaczej wygląda to u prosiąt nowo narodzonych, u których ze względu na niską koncentrację proteaz w jelitach oraz obecność inhibitorów proteaz w siarze działanie toksyny beta może być przyczyną zniszczenia kosmków jelitowych. Towarzyszy temu wydostawanie się krwi do światła jelit. Biegunka bardzo szybko prowadzi do odwonienia i śmierci noworodków. W przypadkach przewlekłych, które nie zdarzają się często, biegunka występuje na przemian z normalnym kałem. Kał biegunkowy jest koloru szarożółtego czasami z domieszką śluzu. Chorujące osobniki mogą padać w okresie kilku dni lub nawet tygodni od zakażenia.
Zapalenie jelit prosiąt wywołane przez Clostridium perfringens typu A
Jak już wspomniano, bakterie z gatunku C. perfringens typu A są normalną składową mikrobiomu jelit. Jednak w sprzyjających warunkach może dojść do nadmiernego ich namnożenia i rozwoju choroby – biegunki. Sprzyjać rozwojowi choroby może przede wszystkim duża ilość C. perfringens typu A w środowisku, co związane jest ze źle prowadzoną dezynfekcją pomieszczeń. Korzystne dla rozwoju choroby jest też uszkodzenie kosmków jelitowych przez rotawirusy czy kokcydia.
Przeciwnie niż w przypadku typu C, adhezja szczepów typu A do kosmków jelitowych nie jest powszechna. Martwica enterocytów po eksperymentalnym zakażeniu wykształca się znacznie rzadziej niż w przypadku typu C. W patogenezie dużą rolę odgrywa przede wszystkim toksyna alfa. Toksyna ta niszczy błony komórkowe enterocytów jelit cienkich, powoduje uszkodzenie bariery jelitowej, wywołuje stan zapalny jelit oraz martwicę, co prowadzi do zaburzeń we wchłanianiu substancji odżywczych. Jak wspomniano, objawy chorobowe występują w zasadzie tylko u prosiąt ssących w pierwszych dniach ich życia.
Objawy kliniczne
Wywoływana przez toksynę alfa biegunka nie jest krwotoczna. Objawy pojawiają się zazwyczaj 48-72 godziny po porodzie, ale zdarzają się przypadki biegunek u noworodków. Bardzo często pierwszym symptomem są występujące u części lub wszystkich prosiąt w miocie wymioty. Kilka godzin później pojawia się żółta, lekko kleista biegunka. Objawy te utrzymują się zazwyczaj 2-3 dni, w tym okresie dochodzi do wyniszczenia organizmu u dużego odsetka prosiąt. Jak wynika z obserwacji własnych, mają miejsce przypadki występowania choroby w 5-7 dniu po porodzie. Zdarza się, że w zakażonej chlewni dwie trzecie miotów, a w tym ponad jedna trzecia prosiąt, określanych jest jako dodatnie w aspekcie wykrycia patogennych toksyn. Mimo tego nie u wszystkich obserwuje się objawy chorobowe ze strony przewodu pokarmowego. Choroba rzadko ujawnia się u prosiąt starszych między 3 a 5 tygodniem życia.
Zmiany sekcyjne
Zmiany chorobowe o charakterze zapalenia są najczęściej zaznaczone w jelicie cienkim, w postaci krwotocznego zapalenia z obecnością strzępków martwiczych błony śluzowej. U prosiąt w postaci przewlekłej dominują zmiany martwicze zlokalizowane na kilkunastocentymetrowym odcinku jelit cienkich. Cechą typową jest zgrubienie i pomarszczenie jelita z naprzemiennie występującymi szarożółtymi, podłużnymi bruzdami i wyniosłościami – tzw. jelito prążkowane.
Badania laboratoryjne
Podstawą diagnozy jest wykrycie toksyn alfa i beta-2 w kale i treści z okrężnicy. Istotnym dla rozpoznania wywołanego przez typ A C. perfringens zapalenia jelit jest izolacja z błony śluzowej jelita czczego i biodrowego dużej liczby drobnoustrojów tego typu, wytwarzających wymienione wyżej toksyny.
Profilaktyka ogólna
Lochy:
1. Konieczne jest wyeliminowanie z paszy dla loch wysokoprośnych i karmiących tak zwanych ciemnych śrut – np. rzepakowej czy słonecznikowej. Nawet niewielki ich dodatek może przyczynić się do ujawnienia problemów z C. perfringens typu A.
2. Ograniczyć należy możliwości intoksykacji loch wysokoprośnych mykotoksynami. W tym celu zalecany jest dodatek do pasz preparatów wiążących toksyny.
Profilaktyka swoista
W Polsce zarejestrowanych jest kilka szczepionek zawierających w swoim składzie zarówno toksoid alfa jak i beta. Szczepionki te należy stosować u loch i przede wszystkim pierwiastek w okresie około 5 i 2 tygodni przed porodem. Tak zwana dawka przypominająca powinna być podawana około 2 tygodnie przed każdym kolejnym porodem.
Terapia
Z doświadczeń własnych wynika, że dobre efekty lecznicze daje stosowanie antybiotyków beta-laktamowych.
Zapalenie jelit prosiąt i warchlaków na tle zakażeń Clostridium difficile
Clostridium (C.) difficile występuje w przewodzie pokarmowym człowieka i zwierząt jako komensal. Posiada fimbrie umożliwiające adhezję do błony śluzowej jelit. Drobnoustrój ten obecnie uważany jest jako ważny czynnik etiologiczny biegunki prosiąt ssących. C. difficile jest częstą przyczyną biegunek u dzieci – noworodków.
Patogeneza
Za rozwój choroby odpowiadają głównie toksyny alfa i beta wytwarzane przez C. difficile. Toksyna alfa powoduje destrukcję struktur występujących w cytoplazmie komórek epitelialnych okrężnicy. Zwiększa przepuszczalność błon komórkowych i powoduje charakterystyczną dla działania enterotoksyn sekrecję płynów do światła jelita. Należy podkreślić, żenie tylko nieracjonalnie stosowane antybiotyki, ale każdy czynnik, który powoduje zaburzenia w równowadze mikrobiomu, czyli w relacjach tworzących ją grup drobnoustrojów sprzyja rozwojowi postaci klinicznej choroby. Drugim ważnym etapem chorobotwórczym jest kolonizacja przez toksynotwórcze szczepy C. difficile błony śluzowej przewodu pokarmowego. Sprzyjają temu wspomniane fimbrie warunkujące adhezję. Trzecią determinantą ujawnienia się procesu chorobowego jest wytwarzanie przez namnożone w dużej ilości komórki C. difficile toksyn: alfa i beta lub jednej z nich.
Objawy kliniczne
Efekty kliniczne infekcji wywołanej przez C. difficile są w swym obrazie chorobowym zróżnicowane. Najczęstszym objawem jest biegunka ujawniająca się u chorych prosiąt. W wyniku infekcji wywołanej przez C. difficile zachorowuje około 30% osesków, a niekiedy wszystkie zwierzęta danego miotu. Śmiertelność w grupach prosiąt odsadzonych jest znacznie niższa, może maksymalnie dochodzić do 15%. Drobnoustrój ten nie jest w stanie wywołać objawów klinicznych u warchlaków czytuczników. U ozdrowieńców przyrosty m.c. są wolniejsze w porównaniu do prosiąt, które nie przechodziły biegunki.
Zmiany sekcyjne
Zmiany patologiczne związane z infekcją C. difficile mogą – rzadko – oprócz okrężnicy występować też w jelicie cienkim.
Badanie bakteriologiczne
Do badań przekazać należy materiał z błony śluzowej okrężnicy. Konieczne jest wykazanie obecności toksyn oraz ocena chorobotwórczości szczepów.
Profilaktyka ogólna
Biorąc pod uwagę przyczyny choroby, konieczne jest ograniczenie stosowania antybiotyków u świń. W paszach dla prosiąt celowe jest podawanie probiotyków blokujących receptory dla C. diifficile (competitive exclusion). Za zasadę uznawać należy stosowanie – najlepiej w wodzie – zakwaszaczy.
Profilaktyka swoista
W Polsce dostępna jest, przeznaczona do immunizacji loch, szczepionka Suiseng DIFF/A zawierająca w swoim składzie toksoidy alfa i beta C. difficile oraz toksoid alfa C. perfringens typu A. Równoczesne zastosowanie tej szczepionki oraz biopreparatu Suiseng coli/C zawierającego antygeny fimbrialne E. coli (F4ab, F4ac F5 i F6 ) oraz toksoid C. perfringens typu C chroni prosięta w zasadzie przed wszystkimi bakteryjnymi przyczynami chorób biegunkowych u prosiąt. Wspomniane biopreparaty w szczepieniu podstawowym należy aplikować samicom prośnym 5 i 2 tygodnie przed porodem. Dawkę przypominającą podawać nie później niż 2 tygodnie przed każdym kolejnym porodem. Warto dodać, że szczepionki te można łączyć i podawać w jednej iniekcji.
Terapia
Nawadnianie prosiąt z objawami biegunki oraz podanie stosownego antybiotyku. Zalecane są: tiamulna, walnemulina i tulatromycyna.
Skutki wczesnego zakażenia prosiąt bakteriami Lawsonia intracellularis
Wywołane przez bakterie Lawsonia intracellularis (L. intracellularis) rozrostowe zapalenie jelit, określane często jako adenomatoza, występuje w zasadzie wyłącznie u tuczników, warchlaków oraz zwierząt stada podstawowego. Bardzo rzadko bakterie te uznaje się za przyczynę problemów zdrowotnych prosiąt. Badaniami laboratoryjnymi wykazano, że już u prosiąt 7-9 tygodniowych można stwierdzić obecność czynnych, czyli wytworzonych przez organizm prosięcia – swoistych przeciwciał skierowanych przeciwko L. intracellularis. Oznacza to, że w niektórych sytuacjach dojść może do wczesnego – około 5 tygodnia życia – zakażenia prosiąt bakteriami L. intracellularis. Badaniami immunohistochemicznymi wykazano, że namnażanie się tych bakterii ma miejsce w enterocytach nabłonka jelit cienkich. Odsetek komórek zakażonych kilka dni po infekcji przekracza 90%. Uwalniany przez bakterie czynnik mitogenny doprowadza do zmian w fizjologicznych procesach komórek gospodarza. Konsekwencją jest powstanie zmian zapalnych w jelicie biodrowym, następnie czczym, ślepym oraz w okrężnicy. Zmiany te mogą prowadzić do rozszczelnienia bariery jelitowej, którą mogą pokonać m.in. znajdujące się w przewodzie pokarmowym paciorkowce, pałeczki okrężnicy i inne drobnoustroje. Powyższe prowadzić może do powstania biegunki na tle zakażeń mieszanych (E. coli + beztlenowce + rotawirusy + cirkowirusy + itd.). Poważniejszą konsekwencją wydaje się być rozprzestrzenienie się w organizmie młodego osobnika patogennych paciorkowców. Widocznym skutkiem tego ostatniego jest mająca różne postacie kliniczne streptokokoza. O istnieniu takiego prawdopodobieństwa dowodzą pośrednio obserwacje terenowe. Niejednokrotnie wykazano, że szczepienie prosiąt w 21 dniu życia po pierwsze ogranicza występowanie biegunek, których etiologia jest wieloczynnikowa, po drugie, zmniejsza zdecydowanie problemy związane ze streptokokozą w grupach prosiąt odsadzonych oraz warchlaków.
Pierwotną przyczyną intensywnego namnażania się L. intracellularis w organizmie odsadzonych prosiąt może być m.in. osłabienie sprawności układu odpornościowego odsadzonych świń. Związane jest to ze stresem odsadzeniowym wywoływanym między innymi odłączeniem osesków od matki, zmianą środowiska przebywania prosiąt czy zmianą paszy. Wszystkie te czynniki mają duży, negatywny wpływ na funkcjonowanie układu odpornościowego. W takiej sytuacji występujące ubikwitarnie (wszędobylskie) drobnoustroje L. intracellularis przy niskim poziomie swoistej odporności biernej mają optymalne warunki do intensywnego namnażania się w przewodzie pokarmowym prosiąt. Skutkami spowodowanych tym zmian zapalnych może być zmniejszenie się „szczelności” jelit i opisane wyżej konsekwencje.
Wykazano, że wczesne szczepienie prosiąt – w 21 dniu życia – odgrywa ważną rolę nie tylko w ograniczaniu występowania adenomatozy u warchlaków i tuczników, ale ogranicza występowanie biegunek prosiąt o etiologii wieloczynnikowej i wyraźnie zmniejsza natężenie występowania streptokokozy.
Wydaje się, że najwygodniejszym, a przede wszystkim skutecznym sposobem ograniczania intensywnego namnażania się Lawsonii w przewodzie pokarmowym jest jednorazowe podanie, w 21 dniu życia szczepionki Porcilis Lawsonia. Alternatywą jest doustne podanie w tym okresie szczepionki Enterisol.
Reasumując, można stwierdzić, że przede wszystkim obserwacje terenowe, a w mniejszym stopniu wyniki badań laboratoryjnych (ze względu na szereg ograniczeń), wydają się wskazywać, że beztlenowce oraz drobnoustroje L. intracellularis, które uznawać należy za normalną składową flory bakteryjnej przewodu pokarmowego, w określonych sytuacjach stają się przyczyną zachorowań. Dotyczy to przede wszystkim noworodków i w mniejszym stopniu prosiąt ssących – w wieku 3-5 tygodni. Przyczyny tego stosunkowo nowego zjawiska są zróżnicowane. Być może intensywny chów świń, coraz mniej oporne na choroby linie genetyczne zwierząt, zmieniające się warunki chowu, istotne ograniczenie występowania takich chorób jak kolibakteriozy oraz zmieniające się sposoby i techniki żywienia świń mają w tym swój udział.
Biorąc powyższe pod uwagę, zwalczanie biegunek prosiąt powinno być wielokierunkowe. Dysponujemy szczepionkami pozwalającymi na ochronę prosiąt przed wszystkimi biegunkami na tle bakteryjnym.
Tabela 1. Czynniki chorobotwórcze biegunek wywoływanych przez beztlenowce
| Nazwa choroby | Czynnik etiologiczny | Chorobotwórcza toksyna | Grupa wiekowa świń | Śmiertelność |
| Zakaźne martwicowe zapalenie jelit prosiąt noworodków | C. perfringens typ C (warunkowo-chorobotwórczy). Rzadko w jelitach. Ograniczone wytwarzanie spor | Β CPB2 adhezja do kosmków | Noworodki 12 godz. – 7 dni | ≈ 50% |
| Zapalenie jelit prosiąt | C. perfringens typ A (niechorobot.). Normalny składnik flory jelit, szczególnie okrężnicy. Ograniczone wytwarzanie spor | Α CPB2 brak adhezji | Prosięta, warchlaki do 3-go miesiąca | 5-20% |
| Zapalenie jelit prosiąt i warchlaków | C. difficile (niechorobotwórczy). Normalny składnik flory jelit. Łatwo wytwarza spory | α, β ADP – rybotransferaza | Prosięta, warchlaki | do 15% |
Tabela 2. Główne toksyny wytwarzane przez różne typy (toksowary) Clostridium perfringens
| Toksotyp | Toksyny | |||
| Alfa (CPB) | Beta (CPB) | Epsilon (Etx) | Jotta (Itx) | |
| A* | + | – | – | – |
| B | + | + | + | – |
| C* | + | + | + | + |
| D | + | – | + | – |
| E | + | – | – | + |
* Produkują też toksyny CPB2
Tabela 3. Objawy kliniczne i zmiany sekcyjne w przebiegu biegunek wywołanych przez beztlenowce
| Nazwa choroby | Objawy kliniczne | Lokalizacja zmian | Zmiany sekcyjne |
| Zakaźne martwicowe zapalenie jelit prosiąt noworodków C. perfringens C | Biegunka, często krwawa, wyniszczenie, niereagowanie na bodźce, w.c.c. 35ºC | Jelito czcze, niekiedy jelito ślepe i okrężnica, zmiany odcinkowe | Stan zapalny, martwica i obrzęk błony śluzowej wyłącznie jelit cienkich, przekrwienie węzłów chłonnych |
| Zapalenie jelit prosiąt C. perfringens A | Biegunka, bez krwi, znaczna domieszka śluzu. Objawy mogą wystąpić u warchlaków | Jelito czcze i biodrowe, początkowy odcinek okrężnicy | Obrzęk błony śluzowej jelit cienkich i okrężnicy, mazista treść o barwie żółtej, brak martwicy |
| Zapalenie jelit prosiąt i noworodków C. difficile | Jelito czcze, biodrowe, niekiedy okrężnica | Toksyczne rozszerzenie światła okrężnicy, wzdęcie |
Tabela 4. Laboratoryjne rozpoznawanie infekcji jelitowych wywołanych przez beztlenowce
| Nazwa choroby | Rodzaj próbki | Warunki przesyłania próbek | Rodzaj testu |
| Zakaźne martwicowe zapalenie jelit prosiąt noworodków C. perfringens C | Podwiązane jelito cienkie lub zeskrobiny z jelita | Próbki w schłodzeniu do badań bakteriologicznych i próbki w buforowanej 10% formalinie do badań histopatologicznych | Badanie bakteriologiczne, w warunkach ściśle beztlenowych, test ELISA w kierunku wykrycia toksyn. Badanie histologiczne; podstawa do podejrzenia w przypadku typu C C. perfringens. PCR |
| Zapalenie jelit prosiąt C. perfringens A | Wymazy na szkiełka podstawowe z błony śluzowej jelita czczego lub biodrowego, nie z okrężnicy!!! | Próbki w schłodzeniu lub zamrożeniu | Badanie bakteriologiczne, ELISA, PCR |
| Zapalenie jelit prosiąt i noworodków C. difficile | Zawartość jelita lub zeskrobiny z błony śluzowej okrężnicy | Próbka schłodzona lub zamrożona do momentu badania; po rozmrożeniu i doprowadzeniu do temp. pokojowej | Bakteriologiczne badanie jakościowe i ilościowe, ocena chorobotwórczości szczepów przy użyciu myszek. PCR, ELISA do identyfikacji toksyn, PCR |
Tabela 5. Profilaktyka i terapia chorób beztlenowcowych świń
| Nazwa choroby | Profilaktyka swoista | Profilaktyka ogólna, terapia |
| Zakaźne martwicowe zapalenie jelit prosiąt noworodków C. perfringens C | Gletvax, Porcilis coli 6C, Colisuin Cl, Enteroporc AC, Suiseng | Mało skuteczna, penicylina, tetracykliny, probiotyki |
| Zapalenie jelit prosiąt C. perfringens A | Szczepionki zawierające anatoksynę α | Lochy: Wycofanie „ciemnych śrut”, eliminacja mykotoksyn z paszy, kontrola zaparć poporodowych, tiamulina, walnemulina, tulatromycyna, zakwaszacze, probiotyki. Prosięta: probiotyki po urodzeniu, zakwaszacze, nawadnianie |
| Zapalenie jelit prosiąt. C. difficile | Suiseng DIFF/A | j.w. |