Lek. wet. Wojciech Bukała,
specjalista chorób trzody chlewnej
MSD Animal Health
Gryzące fakty na temat kanibalizmu
Kiedy świnia gryzie świnię – problem, który hodowcy wolą przemilczeć
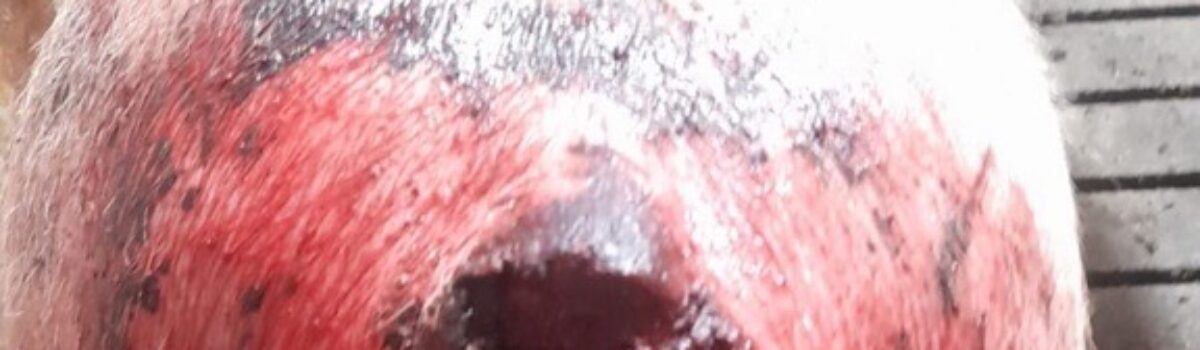
Jest taki moment w chlewni, który każdy doświadczony hodowca zna. Wchodzisz rano do tuczarni i widzisz krew na podłodze. Jedna sztuka stoi w rogu kojca, ogon – a właściwie to, co z niego zostało – wisi jak krwawy strzęp. Pozostałe świnie kręcą się wokół niej z wyraźnym zainteresowaniem. I już wiesz, że jeśli teraz czegoś nie zrobisz, za kilka godzin będziesz miał problem, który wymknie się spod kontroli.
Kanibalizm u świń to temat, o którym branża hodowlana mówi ciszej i rzadziej niż powinna. Nie dlatego, że jest wstydliwy, ani dlatego, że trudno go rozwiązać. Głównie dlatego, że wiele osób wciąż traktuje go jako wypadek przy pracy – coś losowego, czego nie da się przewidzieć, ani systemowo kontrolować. To poważny błąd. Kanibalizm u świń niemal zawsze jest objawem i sygnałem alarmowym dla hodowcy – informacją, że w stadzie coś nie funkcjonuje prawidłowo.
Ten artykuł to próba zrozumienia, dlaczego świnia w ogóle gryzie inną świnię, co się wtedy dzieje w jej głowie i w chlewni, i co naprawdę działa, kiedy już masz problem.
Ewolucja kontra ferma
Żeby zrozumieć kanibalizm u świń domowych, trzeba spojrzeć na ich bliskich krewnych. Dzik europejski żyje w małych, luźno powiązanych grupach rodzinnych, które zasiedlają rozległe terytoria. W ich granicach zwierzęta znajdują pokarm, odpoczywają i realizują pełne spektrum właściwych gatunkowo zachowań. Dzik może ustalić hierarchię bez konieczności walki – wystarczą sygnały zapachowe, wokalizacje, rytualne demonstracje siły. W ostateczności może po prostu odejść, bo ma gdzie.
Świnia fermowa praktycznie nie może prezentować żadnego z tych zachowań. Żyje w grupie nierzadko kilkudziesięciu osobników, ma mocno ograniczoną przestrzeń, stały harmonogram karmienia i często żadnych możliwości eksploracji środowiska. Świnia jest najbardziej inteligentnym zwierzęciem hodowlanym. Zdolności poznawcze mózgu świń są porównywalne ze zdolnościami psami, a nawet 3-4-letnich dzieci. Badania behawioralne nie pozostawiają nam wątpliwości, że te ograniczenia możliwości prezentowania naturalnego behawioru na fermie zwierzę, przetwarza całą dobę i poziom stresu zwiększa się z dnia na dzień.
Gdy napięcie w grupie rośnie i nie ma możliwości naturalnego rozładowania, dochodzi do przekierowania emocji, w tym przypadku agresji, na inne swinie w kojcu. Świnia nie atakuje źródła stresu, bo często nie jest w stanie go zidentyfikować ani zlokalizować. Atakuje to, co ma przed oczami – dosłownie i w przenośni. Ogon sąsiada, ucho, bok, niezdarne nowo narodzone prosię. I tu zaczyna się lawina, bo krew przyciąga inne sztuki. Mechanizm jest prosty: w naturze krew oznacza słabość, a słabość okazję, którą należy wykorzystać. Instynkty, uśpione przez 9 tysięcy lat udomawiania, budzą się błyskawicznie.
Różne twarze kanibalizmu. Nie wszystkie wyglądają tak samo
Kanibalizm bywa postrzegany przez hodowców jako jeden problem. W rzeczywistości obejmuje kilka odrębnych, często współwystępujących zjawisk, które wymagają odmiennego podejścia.
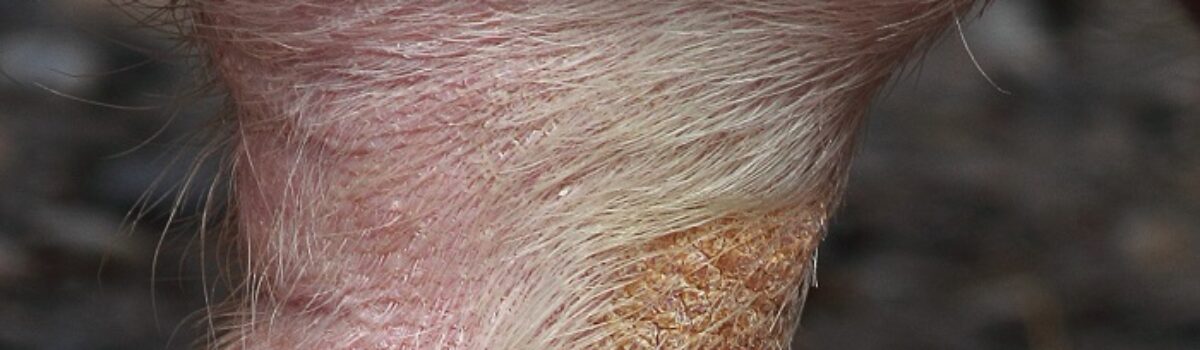
Gryzienie ogonów to najczęstsza i najbardziej rozpoznawalna forma. Zaczyna się subtelnie: lekkie zainteresowanie, węszenie, manipulacja, pierwsze delikatne ugryzienia. Jeśli nikt nie interweniuje, eskaluje błyskawicznie. Uszkodzone tkanki i krew przyciągają kolejne sztuki. W ciężkich przypadkach dochodzi do odsłonięcia kręgów ogonowych, posocznicy i upadków.
Gryzienie uszu często pojawia się już u prosiąt i warchlaków, szczególnie tych odsadzonych zbyt wcześnie. Ucho jest miękkie, łatwo dostępne, silnie unaczynione. Rana wygląda jak z niskobudżetowego horroru z lat dziewięćdziesiątych; dużo krwi, ale rokowanie jest zwykle lepsze niż przy ogonie, o ile zareaguje się szybko.
Gryzienie boków, czyli belly nosing, polega na intensywnym, powtarzalnym trącaniu, a później podgryzaniu brzucha innych zwierząt i jest najczęściej zaburzeniem behawioralnym wynikającym głównie z przedwczesnego odsadzania, braku możliwości ssania oraz niedojrzałości behawioralnej zwierząt. Gryzienie przepuklin to bardziej niepokojąca forma kanibalizmu. Ofiarami są zazwyczaj sztuki z przepuklinami pępkowymi lub mosznowymi – uwypuklona tkanka jest dla zwierząt dość atrakcyjna. Kończy się to często tragicznie, bo wnętrzności eksponowane na zewnątrz nie pozostawiają czasu na reakcję.
Agresja przy porodzie to osobny rozdział. Lochy mogą zagryzać własne prosięta tuż po porodzie – szczególnie jeśli poród był trudny, matka jest pierwiastką albo warunki środowiskowe były złe (chłód, brak materiałów do budowy gniazda). To nie patologia charakteru – to reakcja na stres i ból, ewolucyjny mechanizm „nie inwestuj w potomstwo, którego nie jesteś w stanie wychować”.
Czynniki ryzyka. Co tak naprawdę powoduje, że świnia gryzie świnię?
Gdyby kanibalizm miał jeden, konkretny powód, byłoby łatwo. Problem w tym, że to zjawisko wieloczynnikowe – i właśnie dlatego tak trudno jest je kontrolować w sposób wyrywkowy. Jest wiele czynników, które powodują agresję i kanibalizm – obecnie mówi się nawet o 80 lub więcej.
Zagęszczenie jest numerem jeden na liście czynników ryzyka. Badania są tu jednoznaczne: powyżej pewnego progu obsady na metr kwadratowy agresja rośnie nieproporcjonalnie – nie liniowo, lecz wykładniczo. Świnia potrzebuje przestrzeni nie tylko fizycznej, ale też wizualnej i węchowej. Kiedy każdy ruch jednego osobnika jest natychmiast wyczuwalny przez wszystkie świnie wokół, napięcie nie spada nigdy do zera.
Mieszanie grup to drugi wielki wyzwalacz. Każde wprowadzenie nowych sztuk do istniejącej grupy resetuje hierarchię. Świnie muszą od nowa ustalić, kto jest kim – a ten proces, w warunkach fermowych i bez możliwości ucieczki poza zasięg wzroku, bywa brutalny.
Żywienie to kolejny element układanki, i to w kilku wymiarach. Niedobór lizyny, tryptofanu czy witamin z grupy B może bezpośrednio przekładać się na wzrost agresywności. Tryptofan jest prekursorem serotoniny – hormonu „szczęścia”, który tłumi impulsywną agresję. Świnia z jego niedoborem jest dosłownie biochemicznie bardziej skłonna do ataku. W przebiegu zakażeń jelitowych tj. np. adenomatozy, wskutek uszkodzenia nabłonka jelit i zaburzeń wchłaniania, niedobory te mogą się pogłębiać, dodatkowo obciążając metabolizm zwierząt. Ponadto każde zaburzenie na poziomie jelit, które jest głównym miejscem produkcji serotoniny, powoduje, że w zakażeniach jelitowych dochodzi do obniżenia progu reakcji na stres. Istotną rolę odgrywa też witamina B12, uczestnicząca w tworzeniu krwinek czerwonych i wspierająca prawidłowe funkcjonowanie układu nerwowego. Żywienie to jednak także logistyka: za mała liczba stanowisk paszowych, zbyt krótki dostęp do karmy, rywalizacja o paszę i wodę – każdy z tych elementów generuje napięcie i konflikt.
Mikroklimat jest czynnikiem, który jest nagminnie niedoceniany. Wysoka temperatura i wilgotność – szczególnie latem – nasilają agresję. Świnia w upale jest rozdrażniona, ma wyższe zapotrzebowanie na wodę, gorzej śpi i jest bardziej reaktywna. Paradoks polega na tym, że właśnie latem wentylacja rzadko jest postrzegana jako czynnik behawioralny – przecież kurtyny są podniesione, w budynku wręcz czuć, że wieje. Pamiętajmy jednak, że przeciągi to też jest element, który może powodować agresję u zwierząt.
Monotonia środowiska to problem nowoczesnych, „czystych” chlewni. Im bardziej sterylne i pozbawione bodźców otoczenie, tym bardziej świnia szuka stymulacji – i często znajduje ją w pobratymcu z kojca. Wzbogacenie środowiskowe to dziś nie luksus, ale narzędzie produkcyjne pozwalające realnie kontrolować zachowanie stada.
Ból i choroba mogą wyzwolić zarówno agresję u sprawcy, jak i uczynić ofiarę bardziej podatną. Świnia z kulawizną porusza się inaczej – to wystarczy, by grupa uznała ją za słabą i zaczęła testować jej granice. W praktyce osobnikami często atakowanymi są te najsłabsze i stojące najniżej w hierarchii.
Co czuje ofiara i dlaczego to ważne?
Przez długie lata w hodowli funkcjonowało milczące założenie, że zwierzęta gospodarskie nie odczuwają bólu ani stresu w sposób, który ma znaczenie produkcyjne. Dziś wiemy, że to nieprawda – i to nie jest kwestia sentymentalizmu, lecz nauki potwierdzonej wieloma badaniami.
Świnia ugryziona w ogon lub ucho odczuwa ostry ból. Ten ból powoduje wzrost poziomu kortyzolu, co pogarsza konwersję paszy, obniża odporność i upośledza sen. Ofiara kanibalizmu – jeśli przeżyje – jest przez kolejne dni lub tygodnie wyłączona z optymalnej produkcji. Ale jest też coś więcej: chroniczny stres grupowy, nawet bez widocznych urazów, podnosi bazowy poziom kortyzolu u wszystkich sztuk w kojcu. Cała grupa jest wtedy mniej wydajna, bardziej podatna na choroby, stres, co pogarsza przyrosty.
Kanibalizm ma więc namacalny wymiar ekonomiczny, który wychodzi daleko poza koszt leczenia czy upadku jednej sztuki. To problem, który ciągnie w dół cały kojec, a często całe gospodarstwo.
Interwencja w trakcie. Co robić, kiedy już się dzieje?
Pierwsza zasada: działaj szybko, ale nie panikuj.Kiedy widzisz krew i aktywne gryzienie, pierwszym krokiem jest izolacja sprawcy. Może to brzmieć kontrlogicznie – intuicja podpowiada, żeby ratować ofiarę – ale usunięcie agresora z grupy zapobiega przekierowaniu agresji na inną sztukę.
Zabezpieczenie rany to priorytet. Krew musi zniknąć z pola widzenia jak najszybciej. Używa się do tego preparatów o odpychającym smaku i zapachu, które maskują ranę i zniechęcają do dalszego obgryzania.
Ocena reszty grupy: czy to incydent jednorazowy, czy masz już kilka pogryzionych sztuk? Jeśli więcej niż dwie-trzy – to sygnał, że problem jest systemowy i wymaga interwencji w środowisko, nie tylko leczenia ofiar.
Tymczasowe wzbogacenie jest obowiązkowe. Wrzuć do kojca coś, co odciągnie uwagę zwierząt: łańcuchy zakończone gumowymi zabawkami, sznury, kawałki drewna. Cokolwiek, co da świniom alternatywny obiekt do eksploracji i żucia, które obniżą napięcie i pomogą rozładować stres świń. Ważne, żeby każda sztuka miała łatwy i możliwy dostęp do takich obiektów i żeby zabawki były regularnie wymieniane – inaczej szybko przestają być atrakcyjnym bodźcem. Świnia jako zwierzę inteligentne szybko się nudzi.
Sprawdź parametry, tj.: temperaturę, wilgotność, dostęp do wody i paszy. Często właśnie wtedy hodowca odkrywa, że automat paszowy od trzech dni działa na pół gwizdka albo że jedno z poideł jest zatkane.
Prewencja. Czyli jak nie dopuścić do pierwszego ugryzienia
Tu jest sedno sprawy – i tu jest też największa przestrzeń do działania.
Obsada: Nie ma jednej magicznej liczby, bo wiele zależy od rasy, fazy produkcji i systemu utrzymania. Jeśli regularnie masz problemy z agresją, zacznij od przeglądu obsady. Często okazuje się, że „zawsze tak było” nie oznacza „zawsze tak powinno być.”
Zarządzanie grupami: Im mniej mieszania, tym lepiej. Jeśli musisz łączyć grupy, rób to w neutralnym terenie – w kojcu, który nie należy do żadnej z grup. Daj świniom czas na adaptację w warunkach, które nie faworyzują żadnej ze stron.
Wzbogacenie środowiskowe: Badania jednoznacznie potwierdzają, że świnie mające dostęp do materiałów do rycia i eksploracji rzadziej się gryzą. Słoma jest idealna – daje zajęcie, jest jadalna, można w niej ryć. Tam, gdzie słoma jest niemożliwa (systemy rusztowe), sprawdzają się łańcuchy, gryzaki, sznury jutowe czy konopne lub gałęzie drzew. Kluczowe: materiał musi być nowy, interesujący i możliwy do zniszczenia. Łańcuch wiszący od pół roku przestaje być bodźcem.
Żywienie: Dobrze dobrany poziom tryptofanu i lizyny – skonsultowany ze specjalistą żywienia – przekłada się na wymierne korzyści już w jednym cyklu produkcyjnym. Sprawdź też liczbę stanowisk paszowych: normy mówią o minimum jednym na 8-12 sztuk, ale to minimum, nie optimum.
Monitoring: Regularne, spokojne obserwacje w różnych porach dnia pozwalają wychwycić eskalację napięcia, zanim dojdzie do urazu. Wczesne oznaki to wzmożone węszenie okolic ogonów i uszu, krótkie gwałtowne ugryzienia bez ran oraz wyraźna hierarchizacja przy paszy.
Oświetlenie: Zbyt intensywne lub zbyt długie oświetlenie nasila agresję. Przepisy dobrostanowe wymagają co najmniej 8 godzin światła dziennie o natężeniu nie mniejszym niż 40 luksów. W praktyce wiele chlewni ma oświetlenie włączone znacznie dłużej – i bywa to cichy sprawca problemów, którego łatwo przeoczyć.
Dokowanie ogonów – temat delikatnie pomijany
Skracanie ogonów u nowo narodzonych prosiąt przez lata było najprostszą odpowiedzią na problem gryzienia. Krótszy ogon – mniejszy problem. Skuteczność jest potwierdzona. Problem w tym, że Unia Europejska traktuje ten zabieg jako ostateczność, dozwoloną wyłącznie wtedy, gdy inne metody prewencji zawiodły, i wymaga udokumentowania, dlaczego były niewystarczające. W praktyce wiele krajów i sieci handlowych idzie dalej, żądając chowu zwierząt bez chirurgicznego skracania ogonów, jako warunku współpracy. Jest jeszcze jeden aspekt, o którym praktycznie się nie mówi. Badania histopatologiczne wykazały, że w kikucie ogona, który zostaje po zabiegu dokowania często rozwijają się nerwiaki urazowe, które mogą powodować zwiększoną wrażliwość na ból, a potencjalnie również ból spontaniczny. Oznacza to, że świnia, u której taki nerwiak się rozwinął, może przez całe życie odczuwać przewlekły ból czy dyskomfort w kikucie ogona. Chroniczny ból zaś, jak wiadomo, przekłada się bezpośrednio na poziom stresu i agresywności zwierzęcia oraz jego obniżoną produkcyjność. Skracanie ogonów może więc paradoksalnie współtworzyć ten sam problem, któremu miało zapobiegać.
To zmienia układ sił, ponieważ hodowca, który przez lata rozwiązywał problem elektrycznym lub gazowym nożem, musi teraz zmierzyć się z nim merytorycznie – przez zarządzanie środowiskiem, żywieniem i obsadą. I często okazuje się, że jest to możliwe. Wymaga pracy i nowych inwestycji, ale jest możliwe.
Kiedy wezwać lekarza weterynarii – i co mu powiedzieć?
Wielu hodowców wzywa weterynarza dopiero wtedy, kiedy mają upadki lub ciężko ranne sztuki. To stanowczo za późno.
Lekarz weterynarii powinien pojawić się w chlewni, gdy:
– problem nawraca w tym samym miejscu lub grupie wiekowej, mimo standardowych interwencji,
– liczba poszkodowanych sztuk przekracza 3-5% grupy w ciągu tygodnia,
– pojawia się forma kanibalizmu, której wcześniej nie widziałeś,
– podejrzewasz tło chorobowe — kulawizny, infekcje, niedobory.
Żeby wizyta była efektywna, przygotuj konkretne dane: kiedy problem się pojawił, w której grupie wiekowej, jaka jest obsada, jak wygląda schemat żywienia, jaka temperatura i wentylacja panuje w budynku. Lekarz weterynarii bez tych informacji jest jak generał bez zwiadu – może coś zrobić, ale działanie będzie bardziej intuicyjne niż systemowe.
Świnia nie jest problemem – środowisko jest problemem
Kanibalizm u świń ma opinię problemu nieuchronnego. „Świnie są agresywne, takie są, nic nie poradzisz.” To nieprawda; potwierdza to coraz więcej hodowców, którzy traktują ten temat bardzo poważnie.
Świnia jest zwierzęciem inteligentnym, bardzo społecznym i ciekawskim. W odpowiednich warunkach jest też zaskakująco spokojnym zwierzęciem – znacznie mniej skłonnym do agresji, niż można by sądzić patrząc na warunki, które wiele chlewni wciąż uznaje za standard. Kanibalizm niemal zawsze zaczyna się od środowiska: od zbyt małej przestrzeni, zbyt monotonnego otoczenia, zbyt dużego napięcia przy paszy, zbyt wysokiej temperatury, zbyt intensywnego światła.
Zmień środowisko, a zmienisz zachowanie
To nie jest miękka, sentymentalna filozofia. To twarda ekonomia: mniej urazów, mniej leków, lepsza konwersja paszy, niższy wskaźnik upadków. Świnia, która nie gryzie i nie jest gryziona, rośnie lepiej. A ta dobrostanowa zmiana wzmacnia również reputację wśród odbiorców, którzy coraz częściej uzależniają współpracę od standardów dobrostanu zwierząt.